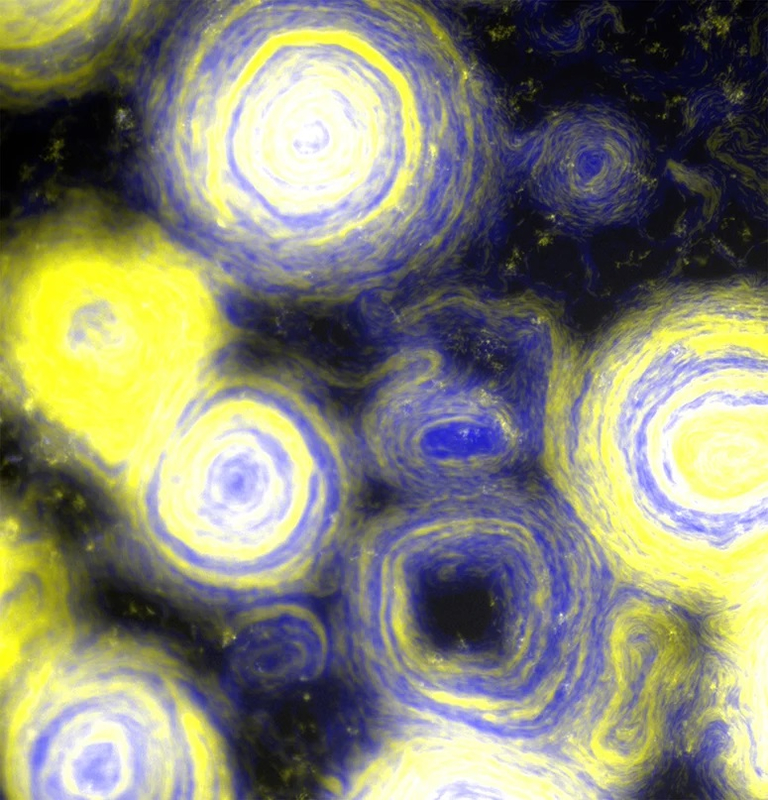
Бактерии-мутанты случайно воссоздали одну из самых знаковых картин Ван Гога
Грань между искусством и наукой иногда бывает зыбкой. Исследователи, изучающие социальную бактерию, которая перемещается и питается скоординированными роями, непреднамеренно воссоздали нечто, очень похожее на знакомый шедевр.
Когда в бактерии, известной как Myxococcus xanthus, сверхэкспрессируется определенный ген, отдельные организмы в течение нескольких часов самоорганизуются в крошечные круговые рои.
После того, как получившиеся рои искусственно окрашиваются, сцена выглядит удивительно похожей на "Звездную ночь" Ван Гога.
"Наша работа показывает, как социальные бактерии, известные как богатые источники терапевтических натуральных продуктов и как агенты биоконтроля сельскохозяйственных культур, служат мощной моделью для изучения эмерджентного поведения, которое также демонстрирует художественную красоту", - говорит микробиолог Дэниел Уолл из Университета Вайоминга.

Бактерии имеют репутацию эгоистов, но M. xanthus называют социальной бактерией, поскольку для выживания ей необходимо находить и узнавать родственников.
После образования больших семейных скоплений эта палочковидная бактерия гораздо лучше нападает на свою жертву, чтобы полакомиться. Каждая клетка вырабатывает пищеварительные ферменты, которые способствуют хищному питанию.
Исследователи уже много лет увлечены этим социальным поведением, но у нас до сих пор нет всеобъемлющей и общепризнанной модели их сложных движений.
В 2017 году Уолл и его коллеги объявили об открытии единственного генетического "переключателя", отвечающего за включение и выключение этого группового поведения.
Этот переключатель специфически контролирует последовательность белков, известную как TraA, которая обеспечивает поверхностный рецептор бактерии для распознавания и прикрепления к рецептору партнера, TraB, на ее родственнике.
После того как бактерия приклеивается к члену семьи через эти два рецептора (TraAB), она может обмениваться питательными веществами и белками с остальными членами группы.
Когда рой сталкивается с пищей, лабораторные исследования показывают, что организмы могут объединять свои ферменты и метаболиты через эти связи, чтобы нанести наиболее мощный удар по своей жертве.
Но все изменилось, когда команда вызвала у мутантных бактерий сверхвыраженные связи TraAB. Именно эта связь позволяет клеткам держаться вместе, но когда этого "социального клея" становится слишком много, рой не может так легко разделиться, чтобы изменить свою форму или направление.
"В нормальных клетках дикого типа они ходят туда-сюда, туда-сюда, туда-сюда, как пригородный поезд", - объясняет биоинженер Олег Игошин из Университета Райса.
"Голова становится хвостом, а хвост - головой. И они делают это каждые 8 минут или около того".
Однако чрезмерная экспрессия TraAB, похоже, останавливает рой от смены головы на хвост и наоборот.
Это то, что, согласно вычислительным моделям, должно произойти, но авторы так и не смогли понять, почему. Насколько они знали, связь TraAB не принимала непосредственного участия в регуляции движения роя, а только в его липкости.
В конечном счете, команда подозревала, что липкость TraB косвенно мешает рою клеток менять направление движения.
"Наша идея заключалась в том, что, возможно, между клетками существует некий сигнал, зависящий от контакта, который подавляет обратное движение", - объясняет Игошин.
"Клетки находятся в плотных группах и постоянно контактируют с другими, но эти контакты преходящи. Но если сверхэкспрессия TraAB действительно делает вас липким, ваш сосед будет оставаться вашим соседом дольше, и это может вызвать сигнал, который подавляет реверсии".
Проверив этот сценарий в вычислительных моделях, авторы смогли подтвердить свою догадку. Всего лишь изменив соединение TraAB, обычные рои "голова к хвосту" внезапно превратились во вращающиеся вихри клеток размером до миллиметра и более.
Дальнейшие эксперименты в лаборатории подтвердили, что это происходит с бактериями и в реальной жизни. В частности, вихри могут возникать, когда штамм чрезмерно выражает липкость, а также когда штамм генетически модифицирован таким образом, чтобы быть непосредственно "нереверсивным".
Результат - не только лучшее понимание того, как миллионы клеток координируют свои движения, но и завораживающая картина микробного мира.
Исследование было опубликовано в журнале mSystems.